Les médicaments ou produits de santé inducteurs enzymatiques peuvent diminuer l’efficacitéde la contraception d’urgence contenant du levonorgestrel (NORLEVO et génériques).
Ces produits, notamment l’éfavirenz (SUSTIVA, ATRIPLA), augmentent le métabolisme du lévonorgestrel et provoquent une réduction des taux plasmatiques du contraceptif.
Selon une étude publiée en 2012 dans la revue Infectious Diseases in Obstetrics and Gynecology,l’administration concomitante d’éfavirenz réduit les taux plasmatiques de lévonorgestrel d’environ 50 %.
En conséquence, les femmes ayant besoin d’utiliser une contraception d’urgence et ayant été traitées par un inducteur enzymatique au cours des 4 dernières semaines doivent recourir à une contraception d’urgence non hormonale (dispositif intra-utérin au cuivre)
Si cette alternative n’est pas possible, la dose standard de lévonorgestrel doit être doublée (3 mg au lieu de 1,5 mg).
Toute grossesse doit en effet être exclue chez les femmes traitées par certains inducteurs enzymatiques du fait qu’ils augmentent le risque de malformation congénitale.

Chez les femmes traitées par un inducteur enzymatique et ayant besoin d’une contraception d’urgence, il est préconisé en 1er lieu un dispositif intra-utérin au cuivre et, en cas d’impossibilité, de doubler la dose de lévonorgestrel (illustration).
L’efficacité de la contraception d’urgence à base de levonorgestrel (NORLEVO et génériques) peut être diminuée par la prise concomitante d’inducteurs enzymatiques, principalement les inducteurs des enzymes CYP3A4.En effet, les inducteurs enzymatiques accélèrent le métabolisme du lévonorgestrel et entraînent une diminution des taux plasmatiques de ce contraceptif.
Cette caractéristique pharmacocinétique de NORLEVO (Cf. Monographie VIDAL – RubriqueInteractions) est observée avec les médicaments et les produits à base de plantes inducteurs des enzymes hépatiques suivants :
- certains médicaments utilisés pour traiter l’épilepsie (comme les barbituriques, la primidone, la phénytoïne ou la carbamazépine) ;
- certains médicaments utilisés pour traiter la tuberculose (comme la rifampicine, larifabutine) ;
- certains médicaments utilisés pour traiter le VIH (comme le ritonavir) ;
- certains médicaments utilisés pour traiter les infections fongiques (comme la griséofulvine) ;
- certains produits à base de plantes (dont des compléments alimentaires) contenant dumillepertuis (Hypericum perforatum).
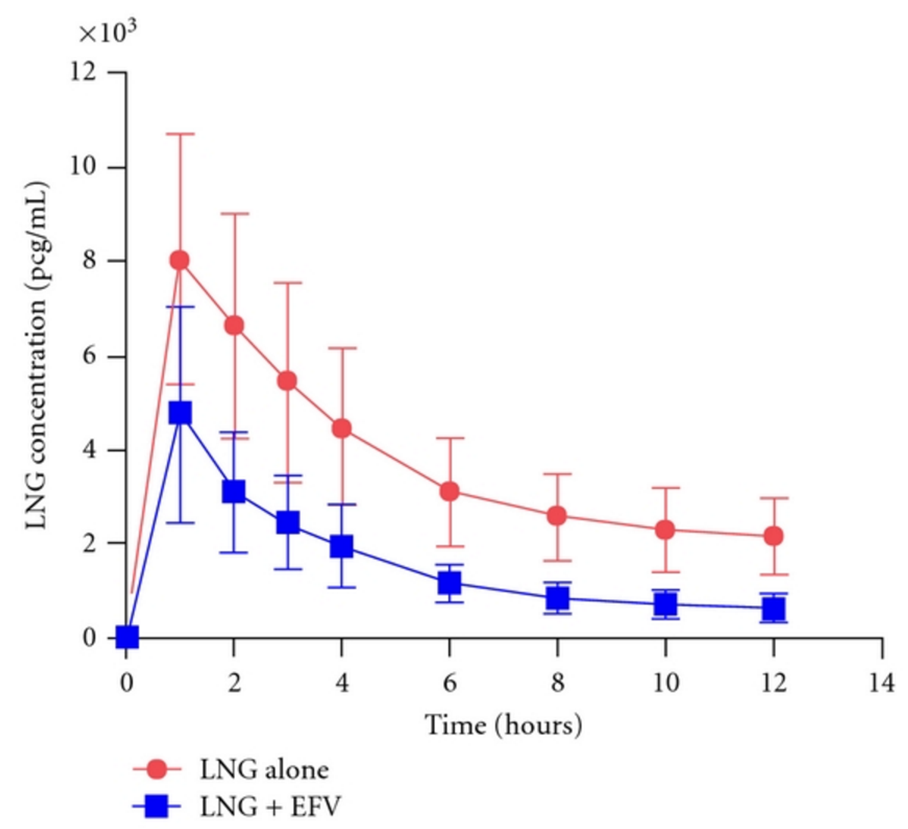
Une étude sur les interactions pharmacocinétiques entre la contraception d’urgence avec lelévonorgestrel et l’inhibiteur non nucléosidique de la transcriptase inverse (INNTI),éfavirenz indiqués dans le traitement du VIH-1 (Carten et al, 2012) a montré qu‘efavirenz réduisait les taux plasmatiques de lévonorgestrel d’environ 50 % (Cf. Figure 1).
 |
Les recommandations de l’ANSM et des laboratoires exploitants
L’exposition à certains inducteurs enzymatiques pendant la grossesse augmente le risque de malformations congénitales. Aussi, est-il recommandé aux femmes traitées par ces médicaments d’exclure toute grossesse et d’avoir recours à une contraception régulière et efficace.
Malgré ces précautions, certaines femmes peuvent avoir besoin d’utiliser une contraception d’urgence, notamment si leur traitement par un produit de santé inducteur enzymatique a eu lieu au cours des 4 dernières semaines.
Dans ce cas, les laboratoires concernés (Cf. Tableau I) préconisent, dans une lettre adressé aux professionnels de santé, d’utiliser une contraception d’urgence non hormonale, à savoir undispositif intra-utérin au cuivre (DIU-Cu).
Le DIU-Cu peut être placé jusqu’à 5 jours après un rapport sexuel non protégé.
Si l’utilisation du DIU est impossible, il est recommandé de doubler la dose standard de lévonorgestrel de 1,5 mg à 3 mg afin de compenser la réduction de la concentration plasmatique du lévonorgestrel.
Les laboratoires indiquent dans leur lettre qu’« une double dose de lévonorgestrel ne devrait pas accroître le risque d’effets indésirables ».
Cependant l’association d’une double dose de lévonorgestrel avec un inducteur enzymatique (médicament ou produit à base de plantes) n’ayant pas été étudiée, il est précisé que tout effet indésirable survenant dans cette situation doit faire l’objet d’une notification de pharmacovigilance.
| Dénomination | Exploitant de l’Autorisation de Mise sur le Marché |
| NORLEVO 1,5 mg, comprimé | Laboratoire HRA Pharma France Information médicale et Pharmacovigilance Tél : 01 53 24 81 00 |
| LEVONORGESTREL BIOGARAN 1500 microgrammes, comprimé | Biogaran Information médicale et Pharmacovigilance Tél : 08 11 907 917 |
| LEVONORGESTREL EG 1,5 mg, comprimé | EG Labo Information médicale et Pharmacovigilance Tél : 01 46 94 86 96 |
| LEVONORGESTREL MYLAN 1,5 mg, comprimé | Mylan S.A.S Information médicale et Pharmacovigilance Tél (service et appel gratuits) : 0800 12 35 50 |
Dans ces situations, l’utilisation concomitante d’inducteurs enzymatiques doit également être prise en compte.
Cette situation peut entraîner une diminution de l’efficacité contraceptive.
Cette interaction est mentionnée dans le résumé des caractéristiques du produit (RCP) de ces médicaments.
NorLevo, Levonorgestrel Biogaran, Levonorgestrel EG, Levonorgestrel Mylan 1,5 mg, comprimé – Contraception hormonale d’urgence contenant du lévonorgestrel : nouvelle recommandation pour les utilisatrices de médicaments inducteurs enzymatiques (ANSM, 17 janvier 2017)
Lettre aux professionnels de santé (sur le site de l’ANSM, 17 janvier 2017)
