Médicament indiqué dans la prévention des nausées et vomissements induits par certaines chimiothérapies chez les enfants et nourrissons âgés de 6 mois à moins de 12 ans, EMEND 125 mg, poudre pour suspension buvable (aprépitant) n’est plus disponible depuis la fin du mois de mars 2026.
Cette situation de rupture d’approvisionnement est consécutive à l’arrêt de commercialisation de cette spécialité par le laboratoire MSD.
Afin d’assurer la continuité de la prise en charge des patients concernés, les autorités sanitaires ont mis en place le dispositif temporaire de remplacement suivant :
1) Remplacement par une alternative adaptée
A la demande de l’ANSM, le laboratoire procède à l’importation des spécialités suivantes :
- IVEMEND 150 mg, poudre pour solution pour perfusion (fosaprépitant), mis à disposition dans les hôpitaux depuis la fin du mois de mars 2026 ;
- EMEND 125 mg, poudre pour suspension buvable, dont une mise à disposition est prévue à compter du mois de juin 2026, tant en ville qu’à l’hôpital. Il convient de noter que les quantités disponibles permettront de couvrir une durée estimée à trois mois de traitement (non renouvelable dans le contexte d’arrêt de commercialisation).
Dans l’hypothèse où ces spécialités ne seraient pas disponibles, il est permis de recourir à une préparation magistrale.
2) Délivrance d’une préparation magistrale
- Modalités de mise en œuvre
En application de la recommandation de remplacement émise par l’ANSM, en cas d’indisponibilité de la spécialité EMEND 125 mg, poudre pour suspension buvable, ou d’une alternative adaptée, le pharmacien est autorisé, à titre exceptionnel et temporaire, à délivrer une préparation magistrale d’aprépitant sous forme de suspension buvable, réalisée à partir de gélules d’aprépitant.
Ce remplacement peut être effectué sans que le patient ne vous présente une nouvelle ordonnance.
Monographie
Les préparations magistrales sont réalisées sous forme de suspension buvable dosée à 20 mg/mL, prête à l’emploi, conformément à la monographie communiquée par l’ANSM. Elles sont délivrées accompagnées de trois seringues orales de volume adapté (une pour chaque administration).
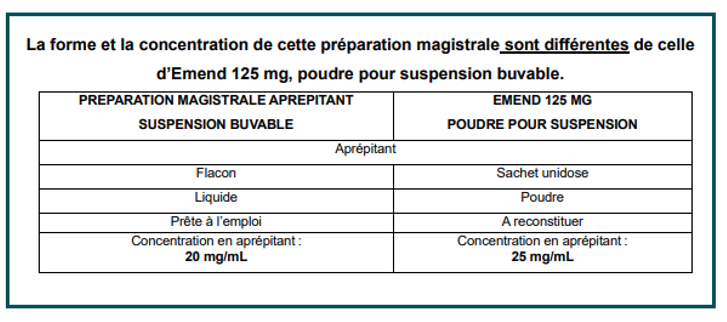
Posologie
La concentration de cette préparation (20 mg/mL) est plus faible que la spécialité EMEND 125 mg reconstituée (25 mg/mL). En conséquence, il convient de vous référer au tableau d’équivalence pour indiquer aux parents ou aidants le volume à administrer selon le poids de l’enfant.
- Modalités de dispensation des préparations magistrales
Lors de la première dispensation d’une préparation magistrale d’aprépitant pour un patient, vous devez obligatoirement informer le prescripteur de ce remplacement par tous moyens appropriés.
Lors de la délivrance de cette préparation magistrale, vous êtes tenus de :
- Informer le parent ou l’aidant du remplacement effectué et lui expliquer de manière claire les modalités de prise de la préparation magistrale, selon le tableau de recommandation de remplacement.
- Remettre au parent ou à l’aidant la fiche d’utilisation de la préparation magistrale d’aprépitant et l’informer de son contenu. Expliquer comment utiliser les pipettes qui sont fournies et préciser qu’elles sont à usage unique.
- Conseiller au parent ou à l’aidant de consulter le médecin ou de contacter le pharmacien en cas de survenue d’effets indésirables ou de symptômes jugés inhabituels, ou encore si le traitement n’agit pas comme d’habitude.
- Inscrire sur l’ordonnance la mention suivante : « préparation magistrale n° (numéro d’ordonnancier) à base d’aprépitant en remplacement de Emend 125 mg, poudre pour suspension buvable, selon la recommandation de l’ANSM » ainsi que le volume de médicament à prélever et à donner à l’enfant.
- Tarification et facturation
Un arrêté publié au Journal officiel du 13 avril 2026 fixe les tarifs de ces préparations, tarifs applicables à compter du 15 avril 2026.
Les préparations magistrales d’aprépitant seront facturées à l’Assurance maladie au moyen d’un code acte « PMR » et seront remboursées à hauteur de 65 %.
Le prix de vente au public de ces préparations magistrales est fixé dans les conditions suivantes :
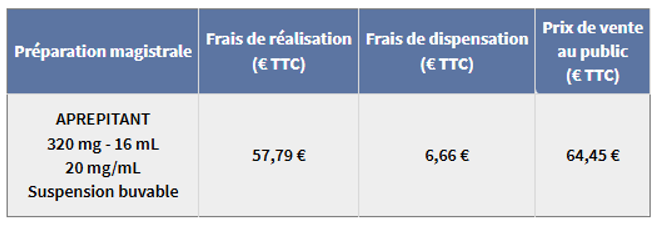
Lors de la dispensation, il convient de dispenser la quantité de principe actif compatible avec la prescription, dans la limite d’un mois de traitement.
Pour aller plus loin :

