Catégorie : Santé Publique
La Cellule de l’InVS PACA CORSE communique:
Dans le cadre de votre activité professionnelle, vous êtes probablement interrogé par vos clients concernant les moyens pour se protéger contre les piqûres de moustiques que ce soit comme nuisant ou au titre de vecteur de maladies (chikungunya et dengue notamment pour Aedes albopictus).
Afin de faciliter le conseil de votre clientèle dans ce domaine, nous vous proposons en pièce jointe un résumé des recommandations actuelles applicables pour les résidents de la région comme pour les voyageurs à destination de zones tropicales.
Vous trouverez également ci-joint la plaquette « Protection anti moustique » destinée à votre clientèle que vous pouvez imprimer à la demande.
Nous espérons que ces éléments vous apporteront une aide dans votre pratique quotidienne.
Vous pourrez trouver :
– des informations complémentaires pour les voyageurs sur : http://www.invs.sante.fr/beh/2014/reco/index.html
– d’autres informations sur Aedes albopictus, le chikungunya et la dengue sur : http://www.ars.paca.sante.fr/Surveillance-epidemiologique-d.141674.0.html
Cordialement.
Florian FRANKE
Epidémiologiste
INSTITUT DE VEILLE SANITAIRE
Département Coordination des Alertes et des Régions
Cellule de l’InVS en Régions Paca et Corse
ARS de Provence-Alpes-Côte d’Azur
132 boulevard de Paris, CS 50039 – 13331 MARSEILLE cedex 03
Tél. : 33 (0)4 13 55 83 19 – Fax : 33 (0)4 13 55 83 47
Les documents importants:
Isotrétinoïne et acitrétine: Délivrance par les pharmacies trop laxistes?
- Médicaments concernés:
- SORIATANE 10mg
- ROACCUTANE 10 mg, capsule molle (ce médicament n’est plus disponible) (princeps)
- ACNETRAIT 10 mg, capsule molle
- CONTRACNE 10 mg, capsule molle
- CURACNE 10 mg, capsule molle
- PROCUTA 10 mg, capsule molle
LE CHIFFRE: Plus de 200 IVG à cause de l’isotrétinoine en 2014!
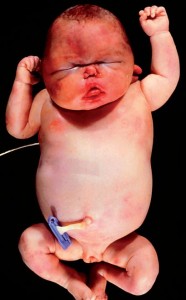 Malgré les renforcements successifs des recommandations concernant la prescription et la délivrance de l’isotrétinoïne chez la femme en âge de procréer, il est clair que toutes les grossesses survenant chez les femmes traitées par isotrétinoïne ne peuvent pas être évitées.
Malgré les renforcements successifs des recommandations concernant la prescription et la délivrance de l’isotrétinoïne chez la femme en âge de procréer, il est clair que toutes les grossesses survenant chez les femmes traitées par isotrétinoïne ne peuvent pas être évitées.
Le manque d’efficacité des différents programmes mis en place pour prévenir ces grossesses est souvent souligné. Ce ne sont pas les programmes qu’il faut remettre en cause, mais leur application.
En effet, la plupart des grossesses exposées en raison de l’absence de contraception ou de la non-réalisation du test de grossesse avant le début du traitement auraient été évitées si le programme avait été appliqué par les professionnels de santé et les patientes.
Ces insuffisances portent autant sur la prescription (absence de contraception ou de prescription du test de grossesse), sur l’information incomplète ou non comprise donnée à la patiente, que sur la délivrance de l’isotrétinoïne qui ne devrait pas avoir lieu lorsque les conditions de prescription ne sont pas toutes respectées.
La mise en place du carnet patiente aurait dû permettre de corriger ces insuffisances, mais ce dernier n’est pas distribué systématiquement à tout médecin, alors que tout médecin peut prescrire de l’isotrétinoïne.
Si l’on veut éviter la survenue de grossesses à risque tératogène élevé et « évitables », il semble indispensable de restreindre la prescription initiale de l’isotrétinoïne aux dermatologues, qui disposent du carnet patiente et qui connaissent mieux les contraintes de sa prescription.
Il semble également nécessaire de conditionner de façon plus stricte la délivrance de l’isotrétinoïne au respect des modalités de prescription définies par l’AMM.
Source © 2014 Société Française de Pharmacologie et de Thérapeutique
NDLR: N’hésitons pas à rappeler à nos équipes les modalités de délivrance de l’isotrétinoïne.
Liste I.
Médicament nécessitant une surveillance particulière pendant le traitement.
Pour les femmes en âge de procréer:
· la prescription nécessite préalablement le recueil de l’accord de soins et de contraception de la patiente et la remise d’un carnet-patiente complété;
· la prescription est limitée à un mois de traitement dont la poursuite nécessite une nouvelle prescription; elle est subordonnée à l’obtention d’un résultat négatif de test de grossesse, qui doit être réalisé tous les mois, dans les 3 jours précédant la prescription; la date et le résultat du test de grossesse doivent être mentionnés dans le carnet-patiente;
· la délivrance doit être effectuée au plus tard 7 jours après la prescription.
· la délivrance ne peut se faire qu’après avoir vérifié que toutes les mentions obligatoires suivantes figurent dans le carnet-patiente:
o lors de la première prescription:
Signature de l’accord de soins et de contraception
Mise en place d’au moins une méthode de contraception efficace depuis au moins un mois
Evaluation du niveau de compréhension de la patiente
Date du test de grossesse (hCG plasmatiques)
o lors des prescriptions suivantes:
Poursuite d’une contraception efficace
Evaluation du niveau de compréhension de la patiente
Date du test de grossesse (hCG plasmatiques)
· la date de délivrance doit être mentionnée dans le carnet-patiente.
source: http://base-donnees-publique.medicaments.gouv.fr/
Autotests de dépistage du VIH
 Information à l’intention des professionnels de santé et des associations (à communiquer à l’équipe officinale)
Information à l’intention des professionnels de santé et des associations (à communiquer à l’équipe officinale)
Date de validation: février 2015
En raison de la commercialisation prochaine des autotests de dépistage de l’infection par le VIH (ADVIH) sur le marché français, la Direction générale de la santé (DGS) a demandé à la HAS de produire un « guide de bonne pratique » d’utilisation des autotests de dépistage du VIH à destination des professionnels en contact avec les usagers ».
Ce document s’adresse aux pharmaciens qui délivreront les ADVIH mais également aux autres professionnels de santé au sens large (médecins, sages-femmes, infirmiers) ainsi qu’aux travailleurs sociaux et aux associations susceptibles d’être impliqués dans des questions de prévention et de sexualité en rapport avec le VIH.
La liste de questions et réponses pratiques proposée a pour objectif de permettre aux professionnels de répondre aux questions des utilisateurs potentiels d’ADVIH et de les accompagner dans leur démarche de dépistage.
Il a été rédigé en collaboration avec les membres d’un groupe d’experts constitué de représentants d’institutions, d’associations et d’organismes impliqués dans la lutte contre le VIH, de pharmaciens, d’un sociologue, d’un médecin généraliste et d’un biologiste (voir Groupe d’experts en fin de document). Les réponses formulées sont fondées sur les éléments présentés dans un argumentaire.
Ce document tient compte de l’état des connaissances sur les ADVIH (avant leur commercialisation sur le marché français) début mars 2015.
______________________________________
Messages clés
-
L’autotest de dépistage du VIH est un outil complémentaire au dispositif de dépistage actuel et il ne doit pas s’y substituer.
-
L’autotest doit résulter d’un choix libre, éclairé et autonome de l’intéressé. Personne ne doit être forcé à réaliser un autotest.
- L’utilisateur d’un autotest de dépistage du VIH doit lire attentivement la notice avant de commencer le test.
- L’autotest de dépistage du VIH fournit un résultat fiable sur le statut sérologique de l’utilisateur d’il y a 3 mois. Ce résultat ne peut être interprété pour le statut sérologique actuel de l’utilisateur qu’en l’absence de comportement à risque ou exposition accidentelle au VIH depuis au moins 3 mois.
- Il ne dépiste pas les autres infections sexuellement transmissibles, ni les hépatites.
- Il faut vérifier la présence de la bande (ou point) contrôle à la lecture du résultat qui permet de s’assurer que le test a été bien réalisé. Il est important de respecter la fenêtre de lecture (environ 20-30 minutes). Avant et au-delà de cette période, le résultat n’est pas fiable.
- Tout résultat positif doit être confirmé par un test Elisa de 4e génération en laboratoire nécessitant une prise de sang en laboratoire ou dans un CDAG/CIDDIST (futurs CeGIDD).
- L’importance d’un traitement précoce en cas d’infection à VIH confirmée doit être soulignée.
- Sida Info Service (0 800 840 800 appel anonyme et gratuit) propose une information sur le VIH et les ADVIH 24 h/24 et 7 j/7. www.sida-info-service.org
- Des évaluations devront être mises en place afin de suivre l’utilisation des autotests de dépistage de l’infection par le VIH.
Les documents importants:
Autotests VIH – Questions / Réponses à l’intention des professionnels de santé
Autotests VIH – Argumentaire scientifique
source HAS
Dossier Pharmaceutique (DP)
Par décret en date du 24 février 2015 (n° 2015-208), les dispositions réglementaires relatives au Dossier Pharmaceutique (DP) ont été modifiées afin d’intégrer audit dossier une sorte de carnet de vaccination.
A cette fin, la durée de conservation des données relatives à la dispensation des vaccins et médicaments biologiques a été portée respectivement à vingt et un ans et trois ans, tandis que la finalité du traitement de ces données a été modifiée respectivement pour permettre :
– une meilleure information des patients quant à leur statut vaccinal ;
– d’assurer la continuité du traitement.



