Cliquez sur les images pour les agrandir.







LA LETTRE DES PHARMACIENS DU 13
Un service gratuit du syndicat général des pharmaciens des Bouches du Rhône
Dans le cadre du Ségur numérique en Santé, les éditeurs de logiciels de gestion d’officine avaient la possibilité, depuis le 2 février 2022 jusqu’au 31 mars, de déposer une candidature pour être référencés “Ségur”. La liste des candidats vient d’être publiée sur le site de l’Agence du numérique en santé (ANS). Une première étape de franchie pour la poursuite du processus.
Douze éditeurs ont respecté cette échéance. Leurs candidatures sont officiellement retenues pour la suite du processus de référencement. Conformément aux textes de l’arrêté, la liste complète est publiée sur le site de l’ANS.
Pour précision, ces éditeurs ne sont encore pas référencés : ils devront se mettre en conformité d’ici le 16 octobre 2022 pour bénéficier du financement de l’Etat. Tout éditeur absent de cette liste ne pourra pas prétendre à un référencement « Ségur » au titre de Logiciel de Gestion d’Officine.
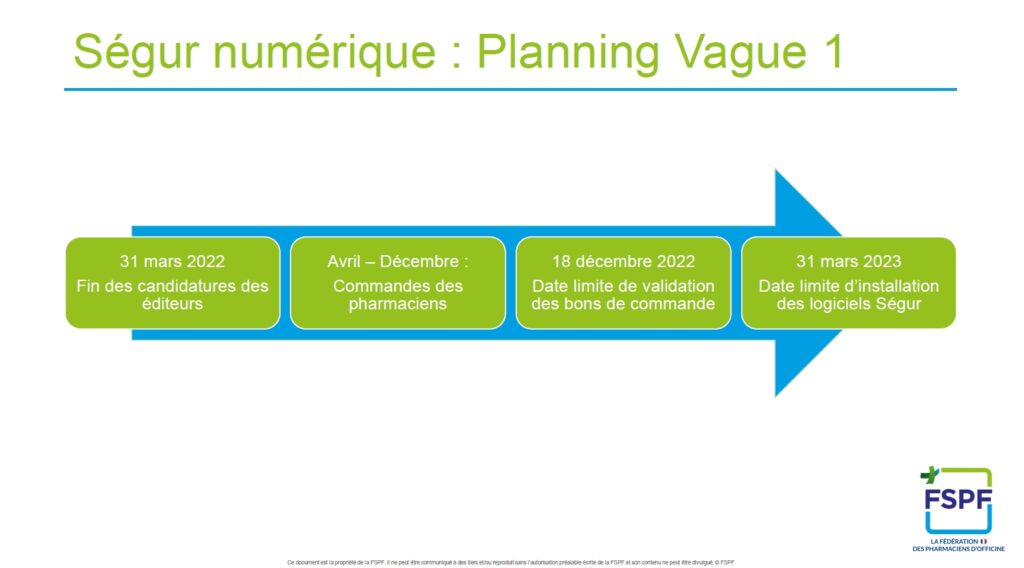
Prochaine étape : après s’être assurés du référencement « Ségur » de leur LGO, les pharmaciens d’officine pourront passer commande, sans frais, de la mise à jour du LGO jusqu’au 18 décembre 2022.
Les évolutions des LGO permettront ainsi d’accéder, par étape :
L’objectif poursuivi est que, dans 12 mois, toutes les officines soient équipées d’un module Ségur vague 1.
> Actualité de l’Ordre du 24 février 2022
> Site de l’Agence du numérique en santé
Dans le cadre du Ségur numérique en Santé, les éditeurs de logiciels de gestion d’officine avaient la possibilité, depuis le 2 février 2022 jusqu’au 31 mars, de déposer une candidature pour être référencés “Ségur”. La liste des candidats vient d’être publiée sur le site de l’Agence du numérique en santé (ANS). Une première étape de franchie pour la poursuite du processus.
Douze éditeurs ont respecté cette échéance. Leurs candidatures sont officiellement retenues pour la suite du processus de référencement. Conformément aux textes de l’arrêté, la liste complète est publiée sur le site de l’ANS.
Pour précision, ces éditeurs ne sont encore pas référencés : ils devront se mettre en conformité d’ici le 16 octobre 2022 pour bénéficier du financement de l’Etat. Tout éditeur absent de cette liste ne pourra pas prétendre à un référencement « Ségur » au titre de Logiciel de Gestion d’Officine.
Prochaine étape : après s’être assurés du référencement « Ségur » de leur LGO, les pharmaciens d’officine pourront passer commande, sans frais, de la mise à jour du LGO jusqu’au 18 décembre 2022.
Les évolutions des LGO permettront ainsi d’accéder, par étape :
L’objectif poursuivi est que, dans 12 mois, toutes les officines soient équipées d’un module Ségur vague 1.
> Actualité de l’Ordre du 24 février 2022
> Site de l’Agence du numérique en santé
source CNOP
Voici un extrait de la présentation de la future CPR (commission paritaire régionale) qui réunira le 29 novembre 2021 les CPAMS régionales et les syndicats pharmaceutiques FSPF (5 membres) et USPO (3membres).
il y a manifestement un problème sur la transmission des RPPS dans le cadre de la télétransmission Sesam-Vital.
P.L


Covid 19 : il est a noter que beaucoup de PS et en particulier de pharmaciens ont reçu , en cette fin d’année, la médaille de l’Ordre du Mérite pour leur gestion de la crise sanitaire.
Tests Covid : environ 8800 pharmacies (sur 21 000) ont vendus 8 M de tests et ont réalisé 3 M de prélèvements. Le 23 décembre les officines françaises ont fait 257 000 tests: la CNAM commence à penser que cela coûte cher!!.
Vaccins grippaux: en 2020, les officines ont réalisé 3,7 M d’actes contre 2,2 M en 2019. Depuis le 1er janvier , s’il nous reste des stocks d’état , on peut les vendre à toute personne qui le demande au prix de 3,01 ttc . Attention, nous ne pouvons vacciner que les personnes cible .
Vaccin Covid : problème sur l’organisation de la livraison ainsi que sur la livraison du matériel d’injection. Suite à la réunion ARS PACA , les pharmaciens fournisseurs d’EHPAD vont recevoir des doses à partir de lundi 18 janvier , ainsi que des seringues ( vérifier que c’est la bonne aiguille !!), du NaCl ( pour reconditionner les doses) et des seringues . Il est urgent que chaque pharmacie s’entende avec son EHPAD pour assurer une livraison immédiate et que les médecins soient près à vacciner . L’arrêté du 30/12/2020 vient de définir une aide de 70 euros par livraison. Il va y avoir une communication pour la vaccination des PS de ville et nos adjoint(e)s et préparat(rices)eurs seront concerné(e)s.
Pour les patients , il faudra une visite médicale de validation puis 2 doses à injecter par le médecin en raison de possibles chocs anaphylactiques (mais surtout lié à une forte pression des syndicats de médecins). La FSPF demande la possibilité de vaccination et, au pire, que nous puissions vacciner au moins pour la 2eme dose.
Sérialisation : il y a un « bruit ministériel » qui court pour essayer de pénaliser les pharmaciens qui ne l’ont pas mise en place . Philippe BESSET s’est insurgé et a bien expliqué qu’il ne laisserait pas faire ( en se servant de voie judiciaire s’il le faut ) . Il faut soit un dédommagement ROSP soit une prise en charge par l’Etat.
L’ avenant 19 signé par USPO qui baisse honoraire HC a été contesté par FSPF en conseil d’Etat qui a donné raison à la FSPF sur 1 point . L’honoraire HC est passé de 1 euro à 0,50 e au 1er janvier 2020 mais le JO l’a enregistré au 04/02/2020 , c’est une perte moyenne de 300 euros par officine que la CNAM doit rembourser !!!
Fermeture des Pharmacies de montagne ou de zones très touristiques : des aides sont prévues. Pour tous , penser à faire la déclaration de perte de CA avant le 15/01/2020.
ECONOMIE:
Nombre d’officines 21 151 au cumul depuis janvier 2020: CA -0,6% AMM R +1,9% non AMM NR +6,3% ( masque test …) marge +1,4%HD -2,5% HC +2,1% ( rappel uspo a signé leur baisse et nous enlève un bon revenu !!) HDR +2,6% HDA +6% HDE +1,8% ( grâce à négo de la fédé)
il est à noter que les HDE rapportent 230Me grâce à FSPF sinon nous aurions une marge négative
CA des génériques augmente car générique hors répertoire augmente et sur des produits chers
L’homéo est déremboursé depuis janvier mais attaquée depuis l’année dernière : -20% en unités et -10M de marge En global, si on regarde l’évolution de la marge réglementée depuis 2015 , on passe de 5,25 Me à 5,24Me en 2019 alors que salaires et charges augmentent
Les demandes de la FSPF sont :
1- augmentation de HDR et retour de HC à 1 euro
2- augmentation de 10% de HD et HG sur générique (et TFR) car la ROSP générique s’effondre
3- pour les petites officines en difficulté et isolée , 1000 euros par mois pour défendre le réseau officinal.
SOINS COORDONNEES:
les négociations ACI CPTS avancent dans le bon sens et vers une simplification. Tous les syndicats y sont favorables ( médecins infirmiers ..) mais ne veulent pas signer avant les élections URPS . Seule USPO est prête à signer . Vote à l’unanimité à la FSPF pour suivre les syndicats des autres professions pour signer tous ensemble car c’est de l’inter pro.
CONVENTION:
ADRI n’a toujours pas amélioré sa fiabilisation qui est de 95% environ ( alors que Visiodroits est à 99,80%). DAD toujours des factures rejetées par sécu , il faut râler auprès de chaque CPAM car c’est eux qui gèrent
PDA toujours rien
TROD COVID attention aux abus sur le prescripteur fictif
Accompagnements pharmaceutiques : il va y avoir des contrôles donc bien garder les justificatifs
ROSP QS (qualité de service) sera à valider à partir du 11 janvier jusqu’au 2 mars 2021
PRALUENT et REPATHA : attention aux ordonnances non conformes ( déclaration obligatoire)
ACTIL veut intégrer Visiodroits ( en cours de signature)
P.L
Si vous voulez en savoir plus sur la sérialisation à l’Officine, nous vous proposons :
Cet outil répond aux principales questions qui nous ont été posées. Il vous permettra, nous l’espérons d’aborder la sérialisation, en toute sérénité.
Comment puis-je être certain que mon système fonctionne correctement ?
Mon lecteur ne lit pas les datamatrix mais que les codes-barres linéaires : que dois-je faire ?
Que dois-je faire avec les boîtes sérialisées ?
Faut-il scanner tous les médicaments ?
Comment m’y retrouver dans mon stock et le gérer ? Comment gérer les prêts ?
Suis-obligé de désactiver les boites sérialisées et à partir de quelle date ?
À quel moment dans mon circuit officinal dois-je scanner les boîtes ?
dD1 – Comment faire pour facturer un médicament promis qui n’a pas été encore scanné ?dD2 – Dois-je scanner un promis qui a déjà été facturé ?dD3 – Le scan d’un médicament modifie-t-il mon processus de facturation si j’ai une alerte ?dD4 – Quand je scanne mon stock est mis à jour : la sérialisation va-t-elle changer quelque chose ?dD5 – Un confrère m’a dépanné d’un médicament. Dois-je le scanner ?dD6 – Un confrère m’a dépanné d’un médicament, je l’ai scanné et j’ai une alerte. Que dois-je faire ?
dE1 – Est-ce que le scan des boîtes est long et va ralentir mon système informatique ?dE2 – Ma connexion Internet ne fonctionne pas tout le temps. Je peux délivrer les boîtes quand même ?dE3 – Si ma connexion internet ne fonctionne pas faut-il scanner les boites quand même ?dE4 – J’ai scanné une boîte sans connexion Internet et j’ai reçu une alerte lorsque la connexion est revenue, or la boite a été délivrée au patient. Que dois-je faire ?
dF1 – Quelles alertes vais-je rencontrer ? Et que faire dans les différents cas de figure ?dF2 – Que dois-je faire si j’ai une alerte de type L5 sur une boîte ? dois-je la retourner à mon grossiste ? La délivrer au patient ?dF3 – Comment me faire rembourser si une boîte déclenche une alerte de falsification potentielle (alerte de type L5) ?dF4 – Qui reprend le produit en cas d’alerte de falsification potentielle (alerte de type L5) ?dF5 – Il y a-t-il une procédure spéciale pour la reprise d’un produit en cas d’alerte de falsification potentielle (alerte de type L5) ?dF6 – La reprise est-elle valable pour tous les produits en cas d’alerte de falsification potentielle (alerte de type L5) ?dF7 – Qui prend en charge financièrement le produit en cas d’alerte de falsification potentielle (alerte de type L5) ?dF8 – Qui reprend le produit en cas d’alerte de falsification potentielle (alerte de type L5) ?
dG1 – L’investigation des alertes de falsification potentielle (alertes L5) auprès de France MVO est-elle obligatoire ?dG2 – La transmission des alertes à France MVO est-elle automatique ou manuelle ?dG3 – Dans quelle délais s’effectue le signalement d’une l’alerte et comment ?dG4 – Il y a-t-il une période de quarantaine pour un produit après une alerte de falsification potentielle (alerte L5) ? Et de quelle durée est-elle ?dG5 – Qui me donne des infos après une alerte ? Dans quelle délais ?dG6 – Que faire si je n’obtiens pas de réponse dans les délais ?dG7 – J’ai une alerte lors de la désactivation ou de la vérification d’un produit (en entrée ou au comptoir). Que dois-je faire ?