Dans une communication en date du 25 mars 2025, la Direction Générale de la Santé (DGS) annonce le maintien de la campagne de vaccination contre le Covid-19 durant le printemps 2025, pour les personnes les plus à risques de formes graves de la maladie.
Quelles sont les personnes concernées ?
Une vaccination supplémentaire contre le Covid-19 pourra être administrée aux personnes dont la protection immunitaire diminue plus rapidement dans le temps, en l’espèce :
- Les personnes âgées d’au moins 80 ans;
- Les patients immunodéprimés, quel que soit leur âge;
- Les résidents des établissements d’hébergement pour personnes âgées (EHPAD) dépendantes et des unités de soins de longue durée, quel que soit leur âge.
Ces personnes pourront recevoir une dose de vaccin contre le Covid-19 dans un délai de trois mois après la dernière injection ou infection au SARS-CoV-2.
Néanmoins, toute personne souhaitant se faire vacciner, même si elle ne fait pas partie de la cible, peut recevoir une injection contre le Covid-19.
Quelles sont les modalités de mise en œuvre du rappel de vaccination contre le Covid-19 durant le printemps 2025 ?
La période de rappel s’étendra du 14 avril au 14 juin 2025. Elle est susceptible d’être prolongée en fonction de la situation épidémiologique.
Les commandes de vaccins contre le Covid-19 se feront via le portail de Santé publique France, selon le calendrier suivant :
- Ouverture du portail de commande : lundi 31 mars et mardi 1er avril 2025 ;
- Livraisons des doses commandées aux officines : jeudi 10 et vendredi 11 avril 2025 ;
- Début de la vaccination : lundi 14 avril 2025.
Quelles sont les modalités de conservation et d’administration des vaccins du stock d’Etat ?
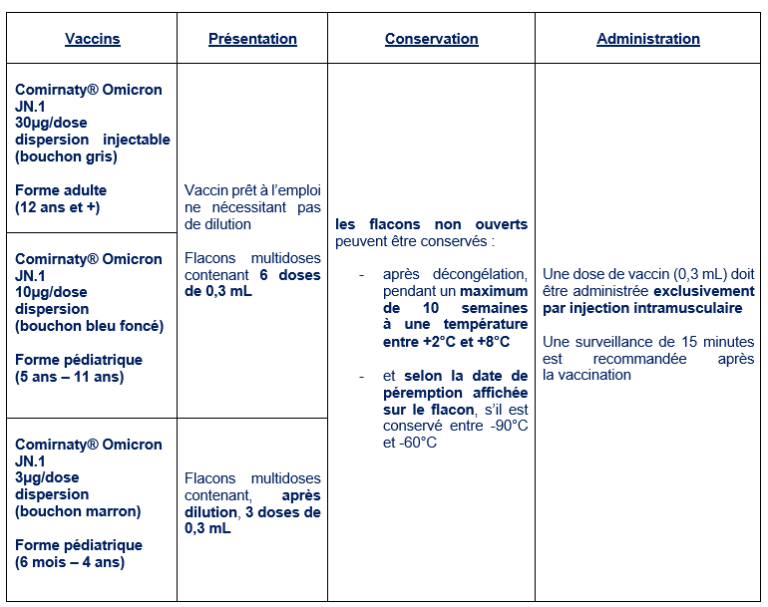
Les flacons peuvent être conservés entre +8°C et +30°C avant la première ponction (incluant le temps de décongélation).
Les boites de vaccins sont dépourvues de notice, mais il est possible d’obtenir le résumé des caractéristiques du produit (RCP) ainsi que des informations complémentaires relatives au bon usage des vaccins :
- en scannant le QR Code présent sur la boîte ;
- en consultant le site internet de l’Agence européenne des médicaments (https://www.ema.europa.eu) ;
- en consultant le site internet du laboratoire (https://www.comirnatyeducation.fr/).
Quelles sont les modalités de commande des vaccins ?
A compter des lundi 31 mars et mardi 1er avril 2025, les pharmacies d’officine pourront commander des flacons du vaccin Comirnaty® de Pfizer-BioNTech pour elles-mêmes et pour les effecteurs autorisés qui leur en font la demande, via l’outil de commande de Santé publique France.
Les vaccins et dispositifs médicaux associés seront livrés selon les délais habituels, entre le jeudi et le vendredi de la semaine suivante, soit à dans un délai de dix jours suivant la session de commande, sauf exceptions.
La pharmacie d’officine peut consulter sa confirmation de commande présentant le détail des quantités commandées et la date de livraison prévisionnelle dès le mercredi suivant la session de commande à partir de 18h00, via l’outil de commande de Santé publique France (dans l’onglet suivi de commande).
La DGS invite les pharmaciens d’officine à prévenir les professionnels de santé pour lesquels elle a commandé des vaccins. Par ailleurs, la DGS recommande aux pharmaciens d’officine de planifier les rendez-vous à partir du lendemain de la date de livraison prévisionnelle indiquée dans la confirmation de commande.
Quelles sont les modalités de facturation applicables ?
Les injections réalisées par les pharmaciens d’officine seront suivies via le code de facturation « INJ ».
Tarif de l’acte d’injection :
– 7,50 euros TTC en France métropolitaine ;
– 7,88 euros TTC dans les départements et régions d’outre-mer (DROM).
Qui peut prescrire le vaccin contre le Covid-19 au sein de l’officine ?
Les pharmaciens d’officine sont compétents pour prescrire le vaccin contre le Covid-19 :
- aux personnes âgées d’au moins 12 ans, à l’exception:
o des femmes enceintes ;
o des personnes présentant un trouble de l’hémostase ;
o des personnes ayant des antécédents de réaction anaphylactique ou présentant des troubles de la coagulation.
- aux enfants âgés de 5 à 11 ans, sauf ceux :
o présentant un trouble de l’hémostase ;
o ayant des antécédents de syndrome inflammatoire multisystémique pédiatrique à la suite d’une infection au Covid-19 ;
o ayant des antécédents de réaction anaphylactique à un des composants du vaccin ou ayant présenté une réaction anaphylactique lors de la première injection.
Les préparateurs en pharmacie et les étudiants en deuxième cycle et en troisième cycle court de pharmacie ne sont pas autorisés à prescrire le vaccin contre le Covid-19.
Qui peut administrer le vaccin contre le Covid-19 au sein de l’officine ?
Les pharmaciens d’officine, les préparateurs en pharmacie et les étudiants en deuxième cycle et en troisième cycle court de pharmacie peuvent administrer le vaccin contre le Covid-19, dans les conditions suivantes :
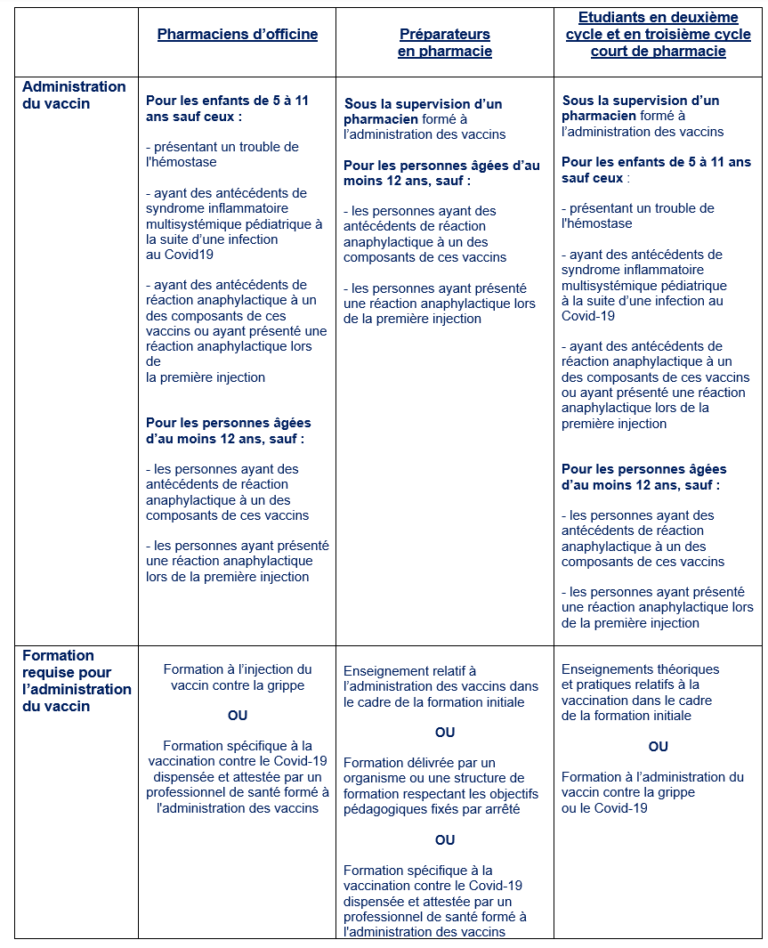
A noter : L’arrêté du 13 février 2025 portant abrogation de diverses mesures de gestion de la crise sanitaire ne remet pas en question la compétence vaccinale des préparateurs en pharmacie et des étudiants en deuxième cycle et en troisième cycle court de pharmacie.
Pour en savoir plus, vous pouvez consulter :
– DGS-URGENT n° 2025-09 du 25 mars 2025 – Covid-19 : renouvellement vaccinal Covid-19 des plus fragiles au printemps 2025 ;
– Haute Autorité de Santé – Avis n°2025.0010/AC/SESPEV du 27 février 2025 du collège de la Haute Autorité de santé relatif à la pertinence de réaliser une campagne de vaccination contre la Covid-19 au printemps 2025.